Aktuelle Compliance-Fristen
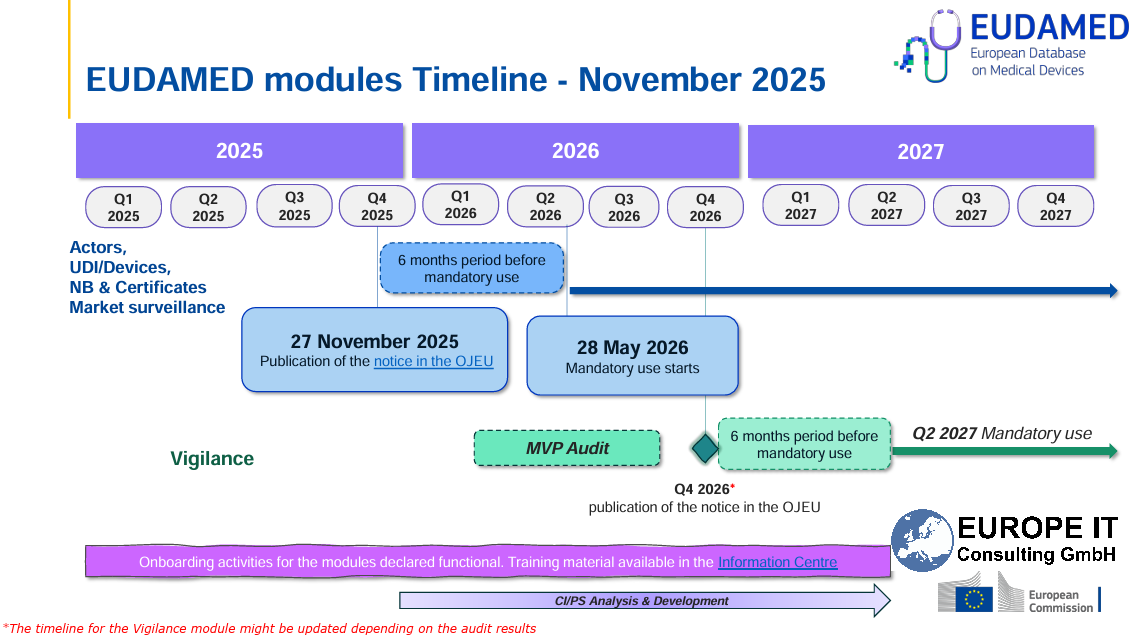
Bleiben Sie konform: Die verpflichtende Nutzung von EUDAMED (EU) für die Registrierung von Medizinprodukten rückt näher. Beachten Sie die aktuellen Übergangsfristen:
Auch in der Schweiz gilt für viele Akteure bereits die Registrierungspflicht über swissdamed (CH). Die parallelen Anforderungen erfordern eine synchrone Strategie:
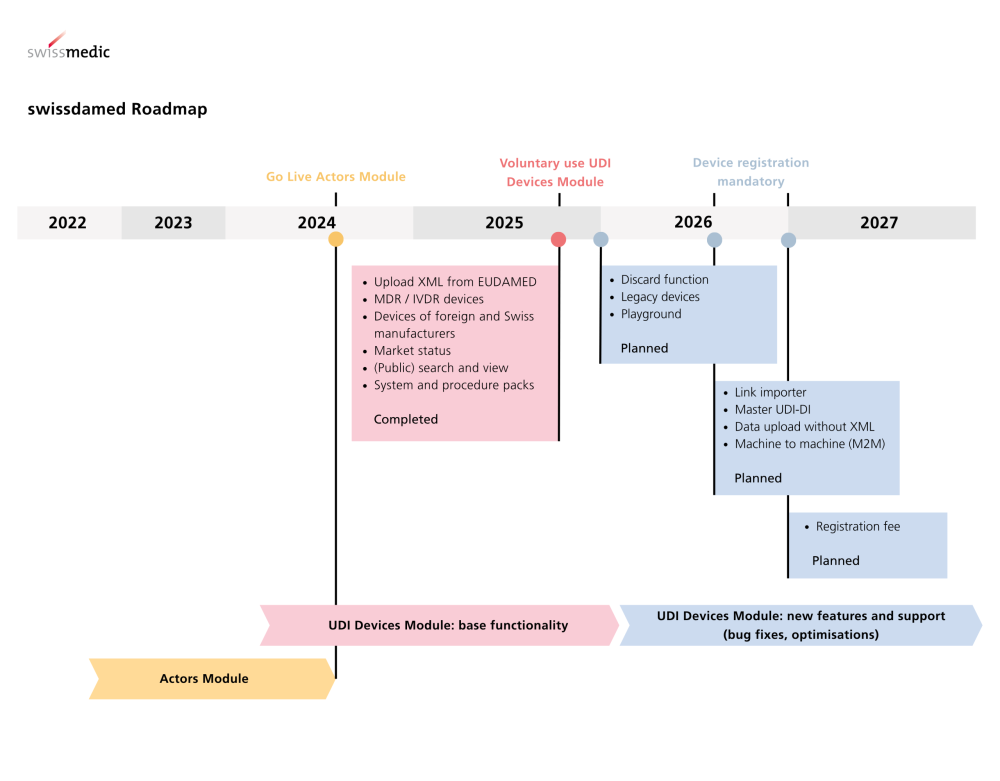
Wir unterstützen Sie dabei, diese beiden Deadlines durch automatisierte Prozesse und unsere kombinierte GSP-Lösung sicher einzuhalten.